Противовирусная терапия хронического гепатита В
Целью проведения противовирусной терапии хронического гепатита В служит профилактика развития цирроза печени,
печеночной недостаточности и печеночно-клеточного рака. Не у всех
пациентов хронический вирусный гепатит В приводит к этим исходам, а если
приводит, то спустя несколько десятилетий после манифестации
заболевания. Именно поэтому для оценки эффективности проводимой терапии
используются более удобные для измерения конечные точки, в число которых
входят подавление репликации вируса, исчезновение е-антигена вируса
гепатита В (HBeAg), исчезновение поверхностного антигена гепатита В (HBsAg), нормализация активности аланинаминотрансферазы
(AЛT) и улучшение гистологической картины печени [1, 2]. Результаты
исследований, в которых приняли участие пациенты, не получающие терапию,
свидетельствуют о стойкой активной репликации вируса гепатита В или
воспалении печени, что отражает высокий уровень репликации ДНК вируса
гепатита В в сыворотке крови, повышение активности AЛT
и выявление HBeAg. Все это указывает на повышенный риск
прогрессирования патологии [3—7]. Таким образом, при определении
показаний для проведения терапии по поводу хронического вирусного
гепатита В необходимо отталкиваться от уровня репликации вируса, а также
активности и стадии патологических изменений в печени [1,8—10]
В течение последнего десятилетия число препаратов, зарегистрированных
для лечения гепатита В, выросло с 1 (интерферон) до 7, в число которых
вошли 5 пероральных аналогов нуклеотидов (нуклеозидов) и 2 интерферона —
стандартный и пегилированный (пегИФН). Доступность лекарственных
средств с мощной противовирусной активностью, безопасных для применения у
пациентов с циррозом и печеночной недостаточностью, расширила
возможности врачей при назначении курса лечения гепатита В. Это в свою
очередь привело к снижению числа пациентов с вирусным гепатитом В,
включенных в лист ожидания на трансплантацию печени [11], а также
увеличило среднюю продолжительность жизни таких больных [12]. Но
несмотря на это остается еще много вопросов, точные ответы на которые не
найдены: 1) когда начинать лечение, 2) какой препарат назначать первым и
3) когда можно отменить терапию. В настоящей статье рассматривается
начальная терапия заболевания. Лечение пациентов с устойчивостью к
противовирусным препаратам описывается в публикации Локарнини (Locarnini
S.) в журнале «Clinics in Liver Disease» № 14, 2010.
Когда начинать терапию
Решение о начале проведения противовирусной терапии пациентам с
жизнеугрожающим состоянием печени, связанным с вирусным гепатитом В, у
которых предполагаемая польза от действия лекарственных средств
существенно преобладает над риском для здоровья, не представляет
затруднений. Сложнее принять такое решение на ранней стадии этого
заболевания, поскольку современные лекарственные препараты не приводят к
эрадикации вируса и большинству пациентов требуется многолетняя, а
иногда и пожизненная терапия с целью предупреждения неблагоприятных
клинических исходов. На схеме 1 приведены показания для назначения
терапии вирусного гепатита В.
Жизнеугрожающее заболевание печени
У пациентов с жизнеугрожающей патологией печени, такой как острая печеночная недостаточность, декомпенсированный цирроз печени
или тяжелое обострение хронического гепатита В, решение о начале
терапии является очевидным. Несмотря на отсутствие рандомизированных
контролируемых клинических исследований противовирусной терапии в
подобных условиях, ее положительные эффекты ранее были
продемонстрированы в когортных исследованиях и сериях клинических
случаев [13, 14]. Эти исследования показали, что противовирусная терапия
обеспечивает стабилизацию функции печени, позволяя пациентам дождаться
трансплантации органа. В некоторых случаях функция печени улучшается до
уровня, позволяющего вычеркнуть таких пациентов из листа ожидания на
трансплантацию. У пациентов, которым предстоит трансплантация печени,
снижение уровня ДНК вируса гепатита В до операции также уменьшает риск
развития рецидива гепатита после трансплантации органа.
Пациенты с жизнеугрожающим повреждением печени должны получать
противовирусную терапию независимо от уровня ДНК вируса гепатита В в
сыворотке и активности АЛТ. При этом лечение должно быть назначено как
можно раньше, поскольку для достижения благоприятного клинического
эффекта может потребоваться от 3 до 6 мес [14].
Компенсированный цирроз
У пациентов с компенсированным циррозом существует риск развития
декомпенсации функций печени или печеночно-клеточного рака. Ключевое
двойное слепое рандомизированное плацебо-контролируемое клиническое
исследование действия ламивудина у пациентов с мостовидным фиброзом или
циррозом и высоким уровнем репликации вируса гепатита В [положительный
HBeAg и/или сывороточный уровень ДНК вируса 700 ООО копий/мл (примерно
140 ООО МЕ/мл)] показало, что терапия ламивудином значимо снижает риск
прогрессирования болезни, определенного как повышение оценки по шкале
Чайлд—Пью (Child-Turcotte-Pugh) на 2 балла и более, начало клинической
декомпенсации или развитие печеночно-клеточного рака [15]. Значимая
разница в первичной конечной точке между опытной и контрольной группами
(7,8 против 17,7%; наблюдалась в среднем через 32,6 мес, что послужило
причиной для независимого комитета по безопасности и мониторингу данных
рекомендовать прекращение исследования. В данном исследовании также была
обнаружена значимая разница между группами по частоте развития
печеночноклеточного рака (3,9 против 7,4%; р=0,047).
Схема 1. Показания для назначения лечения вирусного гепатита В [1]
Лечение однозначно показано:
- Острая печеночная недостаточность
- Цирроз или клинические осложнения гепатита В
- Выраженный фиброз с высоким уровнем ДНК вируса гепатита В в сыворотке крови
- Положительный HBsAg у пациента с запланированной химио- или иммуносупрессивной терапией
Лечение может быть показано:
- HBeAg-положительный или отрицательный хронический гепатит В с активным течением
Лечение обычно не показано:
- HBeAg-положительный хронический гепатит В в фазе иммунотолерантности
- HBeAg-отрицательный хронический гепатит В в фазе неактивного носительства
Полученные данные стали основанием для многих экспертов рекомендовать
противовирусную терапию всем пациентам с компенсированным циррозом.
Однако благоприятные эффекты противовирусной терапии на клинические
исходы у пациентов с компенсированным циррозом и низким уровнем ДНК
вируса гепатита В в сыворотке доказаны не были. Согласно клиническим
рекомендациям Американской ассоциации по изучению заболеваний печени
(AASLD, Association for the Study of Liver Diseases), противовирусную
терапию должны получать пациенты с компенсированным циррозом и уровнем
ДНК вируса гепатита В в сыворотке выше 2000 МЕ/мл [8]. Такая низкая
граница сывороточного уровня ДНК гепатита В была выбрана в связи с тем,
что недавно полученные данные свидетельствовали в пользу связи стойкого
повышения уровня ДНК вируса гепатита В с ростом процента смертности,
обусловленного развитием патологии печени и печеночно-клеточного рака.
При этом риск повышается в случае, если сывороточный уровень ДНК вируса
гепатита В превышает 10 000 копий/мл (-2000 МЕ/мл) [5, 6].
Патология печени без выраженного фиброза
В течении хронического вирусного гепатита В, как правило, выделяют 4
фазы (хотя не у всех пациентов развиваются все фазы, и продолжительность
каждой из них существенно варьирует у разных людей) [16]. Пациентам без
выраженного фиброза противовирусная терапия рекомендуется только в фазе
иммунного клиренса или реактивации, но не в фазе иммунотолерантности
или неактивного носительства. Решение о начале терапии основывается на
репликации вируса гепатита В и активности или стадии патологии печени с
коррекцией на возраст пациента, статус по HBeAg и другие факторы, такие
как мнение самого пациента (рис. 1, 2) [17].
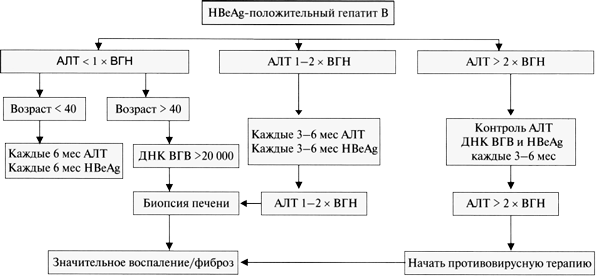
Рис. 1. Алгоритм терапии пациентов с
HBeAg-положительным гепатитом В Здесь и на рис. 2: AJIT —
аланинаминотрансфераза; ВГВ — вирус гепатита В; ВГН — верхняя граница
нормы.
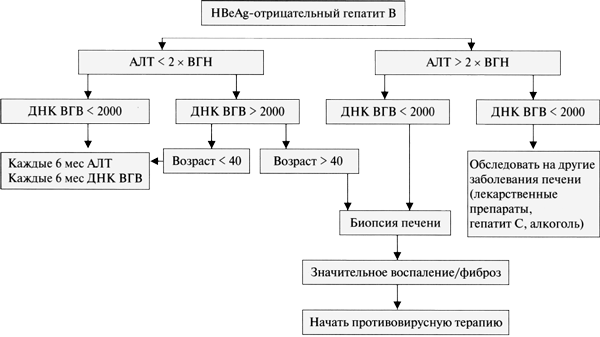
Рис. 2. Алгоритм терапии пациентов с HBeAg-отрицательным гепатитом В
Фаза иммунотолерантносты
Фаза иммунотолерантности характеризуется наличием HBeAg,
нормальной активностью AJIT и высоким уровнем ДНК вируса гепатита В в
сыворотке. В этой фазе проведение противовирусной терапии не
рекомендуется, поскольку у большинства пациентов выявляется небольшое
воспаление с незначительным фиброзом или без такового [18, 19]. Кроме
того, исследования показали, что у пациентов, остающихся в этой фазе,
клинические исходы, равно как и прогрессирование фиброза, выявляются
редко [ 18,20]. Еще одной причиной отсрочки назначения противовирусной
терапии служит ее низкая эффективность в этой фазе. Большинство
исследований показало, что индуцированная терапией (интерферон и аналог
нуклеоз(т)ида) сероконверсия у пациентов с нормальной или несколько
повышенной (в 1—2 раза выше верхней границы нормы) активностью AJIT
встречается редко (<10% случаев после 1 года лечения) [21]. Не так
давно ученые показали, что вирусологический (не определяемый уровень ДНК
вируса гепатита В) или биохимический (нормализация активности AJIT)
положительный ответ на терапию энтекавиром наблюдается лишь у небольшой
доли пациентов с диагностированным HBeAg-положительным гепатитом и
минимальным повышением AJIT (в сравнении с пациентами, у которых
активность AJIT более чем в 2 раза превышает верхнюю границу нормы)
[22]. Таким образом, согласно клиническим рекомендациям, пациенты в фазе
иммунотолерантности должны находиться под постоянным наблюдением.
В нескольких исследованиях было обнаружено, что стойкое повышение
уровня ДНК вируса гепатита В в сыворотке связано с повышенным риском
развития цирроза, печеночной недостаточности и печеночно-клеточного рака
[5, 6, 23]. Однако у большинства пациентов в этих исследованиях не
выявлялся HBeAg, а более половины пациентов были старше 40 лет к моменту
начала сбора данных. В исследовании с долгосрочным периодом наблюдения,
включавшем данные от 508 пациентов с HBeAg-положительным гепатитом,
было обнаружено, что отсроченный клиренс HBeAg у пациентов старше 40 лет
связан с повышенным риском цирроза и печеночноклеточного рака [7]. Эти
данные послужили основанием рекомендовать биопсию печени и назначение
противовирусной терапии пациентам, которые остаются в фазе
иммунотолерантности в возрасте старше 40 лет.
Фаза иммунного клиренса или типичный HBeAg-положительный гепатит
Фаза иммунного клиренса характеризуется наличием HBeAg,
высоким/флуктуирующим уровнем ДНК вируса гепатита В в сыворотке,
персис-тирующим или интермиттирующим повышением активности АЛТ и
наличием признаков некроза и воспаления на биоптате печени. У некоторых
пациентов отмечается спонтанная сероконверсия по HBeAg, при этом
заболевание переходит в фазу неактивного носительства после короткой
фазы иммунного клиренса. У некоторых пациентов могут выявляться
повторяющиеся обострения гепатита с прогрессированием в цирроз или
декомпенсация функции печени, развивающиеся на фоне фазы иммунного
клиренса. Таким образом, согласно клиническим рекомендациям, пациенты в
фазе иммунного клиренса должны находиться под наблюдением врача в
течение 3—6 мес с целью выявления спонтанной сероконверсии по HBeAg [8,
9]. Пациентам, у которых через 3—6 мес сохраняется HBeAg, а активность
АЛТ в сыворотке более чем в 2 раза превышает верхнюю границу нормы,
необходимо назначить противовирусную терапию. В случае обострения с
развитием желтухи или декомпенсации функции печени терапию следует
назначить немедленно.
Фаза неактивного носительства
Фаза неактивного носительства характеризуется отсутствием HBeAg,
стойким сохранением нормальных показателей активности АЛТ и низким или
неопределимым уровнем ДНК вируса гепатита В. Прогноз для пациентов в
случае диагностирования фазы неактивного носительства благоприятный,
особенно если эта фаза наступает в молодом возрасте, до развития
необратимых повреждений печени [24]. Недавние исследования показали, что
у пациентов с высокой нормальной активностью АЛТ (0,5-1 верхней границы
нормы) повышен риск смерти от патологии печени по сравнению с
пациентами с низкой нормальной активностью АЛТ (<0,5 верхней границы
нормы)
Другие исследования также показали, что нарушение работы печени может
наблюдаться у пациентов со стойкими показателями активности АЛТ в
пределах нормы [26, 27]. Однако многие из них основывались на 1 или 2
значениях АЛТ, и в большинстве случаев гистологические исследования
проводились у пациентов с уровнем ДНК вируса гепатита В в сыворотке,
превышающем 4—5 log10 копий/мл. Таким образом, на данный
момент нет существует доказательств в поддержку того, что
противовирусная терапия будет оказывать положительное влияние на
пациентов, которые находятся в фазе неактивного носительства.
Фаза реактивации или HBeAg-отрицательный хронический гепатит
Фаза реактивации характеризуется отсутствием HBeAg, периодическим или
стойким повышением активности АЛТ и уровнем ДНК вируса гепатита В,
который может варьировать от неопределимого до очень высокого (8—9 log10
копий/мл). У большинства пациентов отмечаются преядерные или ядерные
варианты промотера, которые препятствуют или снижают продукцию HBeAg. У
пациентов в этой фазе заболевание часто носит волнообразный характер.
Таким образом, чтобы определить, находится ли пациент в фазе неактивного
носительства или перешел в фазу реактивации, необходимо его регулярное
обследование. Лечение необходимо назначать, как только появятся данные о
том, что у пациента именно хронический HBeAg-отрицательный вирусный
гепатит В, поскольку при этом у многих выявляются прогрессирующие
повреждения печени. Стойкая спонтанная ремиссия наблюдается редко.
Другие факторы, которые необходимо учитывать
На время проведения терапии вирусного гепатита В могут влиять и
другие факторы. Одним из них служит возраст (суррогатный показатель
продолжительности инфекции). Особенно это касается пациентов с
HBeAg-положительным гепатитом при нормальном или минимальном повышении
активности AJIT. Еще одним важным фактором у молодых женщин служит
планирование беременности. Несмотря на то что 2 зарегистрированных
аналога нуклеоз(т)идов относятся к препаратам класса В (телбивудин и
тенофовир), данные о безопасности проведения противовирусной терапии в I
триместре беременности ограничены. В Регистре беременных, получающих
антиретровирусную терапию (Antiretroviral Pregnancy Registry), с 1989 г.
идет отслеживание исходов для матери и плода у женщин, получающих
пероральные нуклеоз(т)иды. На июль 2009 г. были получены данные о 10 803
случаях беременности, в течение которых мать принимала пероральные
аналоги нуклеоз(т)идов по поводу вирусного гепатита В или ВИЧ-инфекции
[28]. Врожденные пороки развития у детей, контактировавших с
ламивуди-ном в I триместре беременности, были выявлены в 2,9% случаев
(96 из 3314), а у детей, контактировавших с тенофовиром — в 2,4% случаев
(18 из 756). Эти показатели сопоставимы с таковыми в контрольной
популяции. Однако зарегистрированы были только данные о живорожденных.
Частота спонтанных абортов и влияние контакта с нуклеоз(т)идами на рост и
развитие ребенка изучены не были.
Данные о риске развития врожденных пороков, связанных с энтекавиром,
адефовиром и телбивудином, ограничены по причине малого числа
зарегистрированных живорожденных. Противовирусная терапия рекомендуется
женщинам с жизнеугрожающей патологией печени и компенсированным циррозом
с высоким уровнем ДНК вируса гепатита В в сыворотке. Для пациенток без
выраженного фиброза решение о назначении противовирусной терапии должно
приниматься с учетом планируемой беременности, ожидаемой
продолжительности терапии и вероятности спонтанного улучшения. Так,
например, у пациенток с HBeAg-положительным гепатитом с минимальным
повышением активности AЛT можно отложить терапию по причине
благоприятного краткосрочного прогноза и необходимости проведения
многолетней терапии для достижения сероконверсии по НBeAg. Все пациентки
должны находиться под наблюдением для своевременного начала терапии в
случае более активного течения гепатита.
В некоторых исследованиях сообщается о семейной группировке случаев
печеночно-клеточного рака. Между тем, какие факторы — генетические,
вирусные или факторы окружающей среды — вносят вклад в семейную
группировку печеночноклеточного рака и как оценить его риск в случае
семейного анамнеза, неизвестно. Несмотря на то что назначение
противовирусной терапии пациентам с хроническим гепатитом В и семейным
анамнезом печеночно-клеточного рака представляется обоснованным, нет
данных в поддержку благоприятных клинических эффектов такого подхода у
пациентов, в остальном не отвечающих критериям назначения терапии.
У пациентов с хроническим гепатитом В, получающих иммуносупрессивную
терапию или химиотерапию по поводу других заболеваний, есть риск
обострения гепатита по причине реактивации репликации вируса гепатита В
[29]. Профилактическая противовирусная терапия рекомендуется всем
пациентам с HBsAg-положительным гепатитом, нуждающимся в долгосрочной
иммуносупрессивной терапии. Реактивация репликации вируса гепатита В
также возможна у пациентов с HBsAg-отрицательным гепатитом, но наличием
антител к ядерному антигену вируса (анти-НВс антитела). Однако риск при
этом существенно ниже [30]. Несмотря на ограниченность данных,
большинство экспертов рекомендуют проведение профилактической
противовирусной терапии пациентам с HBsAg-отрицательным,
анти-НВс-положительным гепатитом, которым предстоит терапия высокого
риска (химиотерапия по поводу злокачественных гематологических
заболеваний или трансплантации костного мозга; назначение ри-туксимаба
по любой причине; долгосрочная терапия глюкокортикоидами).
Что применять для стартовой терапии?
Как только принято решение о начале терапии, следующий вопрос, на
который необходимо ответить, — какой препарат назначить. Решение об
использовании аналога нуклеоз(т)ида или интерферона основывается на
характеристиках и предпочтениях пациента. В табл. 1 представлены все
«за» и «против» терапии интерфероном и аналогами нуклеоз(т)идов. Терапия
интерфероном не рекомендуется пациентам с декомпенсацией функций
печени, иммуносупрессией либо соматическими или психиатрическими
противопоказаниями. Основным преимуществом интерферона служит
ограниченная продолжительность его назначения. Интерферон также
характеризуется более высокой частотой случаев исчезновения HBsAg, хотя
этот положительный эффект преимущественно наблюдается у пациентов,
инфицированных вирусом с генотипом А. В некоторых исследованиях было
обнаружено что сероконверсия по HBeAg, вызванная интерфероном, более
продолжительна, чем вызванная нуклеозидом, но прямые сравнения не
проводились. Основными недостатками интерферона служат необходимость
парентерального назначения и высокая частота развития побочных эффектов.
Нуклеоз(т)идные аналоги назначают внутрь и отличаются очень хорошей
переносимостью. Тем не менее в случае их отмены нередко развиваются
обострения, что требует проведения длительной терапии, а это чревато
развитием устойчивости к противовирусным препаратам.
|
Таблица 1. Сравнительная характеристика терапии интерфероном-а и аналогами нуклеоз(т)идов
|
| Терапия |
ИФН-а |
Аналоги нуклеоз(т)идов |
| Путь введения |
Подкожный |
Пероральный |
| Продолжительность терапии |
Ограниченная (12 мес) |
От нескольких лет до пожизненной |
| Противовирусная активность |
Средняя |
Сильная, зависит от препарата |
| Исчезновение HBsAg |
1-3% через 1 год |
0-1% через 1 год, варьирует в зависимости от препарата |
| Устойчивость |
Нет |
0-25% через 1 год |
| Побочные эффекты |
Частые |
Редкие |
|
Терапия аналогами нуклеоз(т)идов
Аналоги нуклеоз(т)идов, назначаемые при гепатите В, делятся на 3
группы: L-нуклеозиды, включая ламивудин и телбивудин; нециклические
фосфонаты нуклеозидов, включая тенофовир и адефовир; и аналоги
дезоксигуанозина, включая энтекавир. Мутации, возникающие в результате
применения препарата одной группы, приводят, по крайней мере, к
некоторой устойчивости организма к другим препаратам этой группы, в
некоторых случаях снижая чувствительность и к препаратам других групп.
Выбор лекарственного средства для начальной терапии должен основываться
на противовирусной активности и риске развития устойчивости к препарату.
В табл. 2 приводится сравнение частоты ответа, а также устойчивости
организма к 5 зарегистрированным аналогам нуклеоз(т)идов. Энтекавир,
телбивудин и тенофовир обладают более мощной противовирусной
активностью, несколько меньше у ламивудина и затем адефовира. Энтекавир и
тенофовир имеют более высокий генетический барьер развития устойчивости
(частота развития устойчивости к препарату ниже), затем следуют
адефовир, телбивудин и ламивудин. Гистологическим улучшением считали
снижение оценки по шкале некроза и воспаления на >2 балла и
отсутствие ухудшения по шкале фиброза.
Все 5 зарегистрированных аналогов нуклеоз(т)идов характеризуются
хорошей переносимостью, но, как и при использовании других аналогов
нуклеоз(т)идов, существует потенциальный риск развития митохондриальной
токсичности и лактат-ацидоза. О необходимости сохранять бдительность
свидетельствует недавнее изъятие с рынка клевудина, в число побочных
действий которого вошли митохондриальная токсичность и мио-патии [31,
32]. Нефротоксическое действие адефовира и тенофовира было выявлено у 3%
пациентов через 3—5 лет непрерывного назначения [33, 34]. При этом
наблюдалось развитие дисфункции почечных канальцев, синдром Фанкони
(Fanconi). Применение телбивудина на протяжении более чем 3 лет
сопровождалось миалгией/миозитом и периферической нейропатией у 1,4 и
0,28% пациентов соответственно. Риск развития периферической нейропатии
существенно возрастал у пациентов, получавших комбинированную терапию
телбивудином и пегинтерфероном (18,75%) [35, 36]. Недавнее исследование
показало, что назначение энтекавира пациентам с декомпенсацией функций
печени сопровождается высокой частотой развития лактат-ацидоза [37].
Аналоги нуклеоз(т)идов наилучшим образом подходят пациентам с
декомпенсацией функции печени, противопоказаниями к назначению
интерферона и пациентам, согласным на длительный прием препарата. Из 5
зарегистрированных препаратов наилучшим профилем эффективности,
безопасности и лекарственной устойчивости обладают энтекавир и
тенофовир. Энтекавир предпочтительнее назначать пациентам с повышенным
риском развития почечной недостаточности, а тенофовир — молодым женщинам
(в том числе желающим забеременеть), а также пациентам, получавшим в
прошлом ламивудин. Ламивудин и телбивудин не следует назначать при
проведении первой линии терапии по причине высокой частоты лекарственной
устойчивости. Адефовир практически полностью вытеснен тенофовиром из-за
слабой противовирусной активности.
Интерферон
Интерферон противопоказан пациентам с декомпенсированным циррозом
печени по причине риска развития тяжелого сепсиса и прогрессирования
печеночной недостаточности [38, 39]. Также не рекомендуется назначать
его пациентам с тяжелыми обострениями хронического вирусного гепатита В,
острой печеночной недостаточностью и пациентам, получающим
имму-носупрессивную или химиотерапию. Интерферон можно назначать
пациентам с компенсированным циррозом, нормальной синтетической функцией
печени и отсутствием признаков портальной гипертензии. В крупном
регистре клинических исследований пегИФН-а2а наблюдались всплески
повышения активности АЛТ (>5 раз выше верхней границы нормы), которые
не приводили к печеночной декомпенсации, несмотря на то что у 18%
пациентов с Н BeAg-положительным и 31% пациентов с HBeAg-отрицательным
гепатитом, получавших монотерапию пегИФН, был выявлен выраженный фиброз
или компенсированный цирроз [40, 41].
|
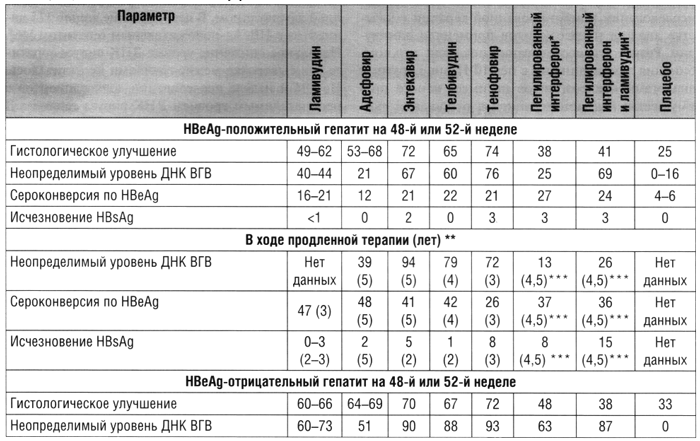
Таблица 2. Частота ответа на терапию зарегистрированными препаратами НВеАд-положительного и НВеАд-отрицательного гепатита В* [2]
|
 |
|
Примечание. ВГВ — вирус гепатита В; * —
биопсию печени выполняли на 24-й неделе после прекращения терапии; ** —
временная точка, в которой оценивали ответ в годах; * * * — оценку
проводили после отмены терапии.
|
В нескольких исследованиях проводилось изучение прогностических
факторов положительного ответа на терапию пегилированным интерфероном с
целью более точного выбора группы пациентов. В ретроспективном анализе
обобщенных данных о 721 пациенте, включенном в 2 исследования пегИФН 111
фазы, прогностическими факторами положительного ответа на терапию у
пациентов с Н Be Ag-положительным гепатитом были высокая активность
AJ1T, низкий уровень ДНК вируса гепатита В, женский пол, более пожилой
возраст и отсутствие предшествующей терапии интерфероном. Наилучшие
исходы были достигнуты у пациентов, инфицированных вирусом с генотипом
А, высокой активностью AJ1T или низким уровнем ДНК вируса, а также
пациентов, инфицированных вирусами генотипа В или С с высокой
активностью AJIT и низким уровнем ДНК вируса [42].
Интерферон отличается от аналогов нуклеоз-(т)идов тем, что он
обладает иммуномодулирую щим и противовирусным эффектом, что может
обеспечивать более высокую частоту исчезновения HBsAg и более
продолжительную вирусную супрессию [42, 43]. Спустя 3 года после лечения
у 28% пациентов с HBeAg-отрицательным гепатитом, получавших пегИФН,
уровень ДНК вируса гепатита В составил 10 000 копий/мл и менее против
15% пациентов, получавших лами-вудин (/7=0,039). Кроме того, у 8,7%
пациентов, получавших пегИФН, было выявлено исчезновение HBsAg. В группе
ламивудина подобный эффект не был достигнут ни у одного из пациентов
[43].
Эти данные свидетельствуют о том, что лучшими кандидатами для терапии
интерфероном служат молодые пациенты без сопутствующих соматических или
психиатрических заболеваний, отказывающиеся от длительного приема
препаратов. У пациентов с HBeAg-положительным гепатитом следует
учитывать генотип вируса и назначать интерферон в случае, если выявлен
генотип А [42].
Комбинированная терапия
Комбинированная терапия была предложена на случай развития аддитивной
или синергичной противовирусной активности, а также в целях
профилактики развития устойчивости к противовирусным препаратам. В
большинстве клинических исследований комбинированной терапии в качестве
аналога нуклеоз(т)идов применяли ламиву-дин. Результаты исследований
показали, что комбинация ламивудина ни с пегИФН, ни с другими аналогами
нуклеоз(т)идов не имеет явного преимущества над монотерапией в отношении
скорости и степени вирусной супрессии. Основным преимуществом этих
комбинаций служит снижение частоты развития устойчивости к ламивудину.
Устойчивость к энтекавиру или тенофовиру при проведении монотерапии
возникает редко.
Комбинация пегИФН и аналога нуклеоз(т)ида
По сравнению с монотерапией пегИФН добавление ламивудина приводило к более выраженной вирусной супрессии.
>Но это преимущество не сохранялась после прекращения терапии [40,
41, 44]. Комбинация пегИФН и ламивудина также сопровождалась более
низкой частотой развития устойчивости к ламивудину по сравнению с
монотерапией лами-вудином, при этом устойчивость к ламивудину не
наблюдалась у пациентов, прошедших курс монотерапии пегИФН. Клиническое
исследование комбинированной терапии пегИФН и телбивудином было
прекращено по причине более высокой частоты развития периферической
нейропатии. В настоящее время продолжаются клинические исследования
комбинированной терапии пегИФН и энтекавиром с одновременным или этапным
назначением 2 препаратов и различной продолжительностью приема
энтекавира.
Комбинированная терапия нуклеоз(т)идами
Все зарегистрированные в настоящее время пероральные препараты,
назначаемые для лечения гепатита В, действуют на полимеразу вируса.
Кроме того, мутации, вызывающие устойчивость к одному препарату, могут
также повлиять на развитие устойчивости к другим. Проведенные до
настоящего времени клинические исследования комбинированной терапии
аналогами нуклеоз(т)идов показали отсутствие аддитивной или синергичной
противовирусной активности и снижение (но не полное исчезновение)
устойчивости к ламивудину.
Исследование II фазы, сравнивающее действие комбинации телбивудина и
ламивудина с монотерапией телбивудином или ламивудином, показало, что
комбинированная терапия обладала такой же или меньшей эффективностью,
чем монотерапия телбивудином [45]. Такой результат, вероятно, обусловлен
тем фактом, что телбивудин и ламиву-дин представляют собой L-нуклеозиды
и мутации против одного препарата вызывают перекрестную устойчивость к
другому.
В другом исследовании сравнивалось действие комбинации ламивудина и
адефовира с монотерапией ламивудином. В исследование вошло 115 пациентов
с HBeAg-положительным гепатитом [46]. Начальное снижение уровня ДНК
вируса гепатита В в сыворотке между группами не отличалось. На 104-й
неделе исследования доля пациентов с неопределимым уровнем ДНК вируса
гепатита В в сыворотке и сероконверсией по HBeAg также была
сопоставимой. У пациентов в группе комбинированной терапии отмечалась
значительно меньшая частота устойчивости к ламивудину (15%), чем в
группе монотерапии ламивудином (43%). Высокая частота устойчивости к
ламивудину в группе комбинированной терапии была неожиданной и,
вероятно, связана со слабой противовирусной активностью адефовира.
Наблюдение пациентов во время терапии
Наблюдение пациентов в ходе терапии позволяет оценить ответ на
лечение, переносимость препарата и приверженность лечению. Все пациенты
во время проведения терапии и, по крайней мере, в течение 24 нед после
ее отмены должны находиться под пристальным наблюдением врача на случай
возможного обострения гепатита (обусловленного реактивацией вируса), что
требует немедленного возобновления лечения. Долгосрочное наблюдение
необходимо для выявления поздних обострений, оценки продолжительности
ответа и частоты исчезновения HBsAg. Наблюдение на предмет
печеночно-клеточного рака должно проводиться в соответствии с
клиническими рекомендациями даже у пациентов с сохраняющейся на фоне
терапии вирусной супрессией или стойким вирусологическим ответом после
ее отмены.
Пациенты, получающие пегилированный интерферон, должны проходить
клинический осмотр с интервалом раз в 12—24 нед. Общий анализ крови и
функциональные печеночные тесты следует выполнять сначала каждые 4, а
затем каждые 4—12 нед. Каждые 12 нед следует определять уровень ДНК
вируса гепатита В в сыворотке. Уровень тиреоидных гормонов контролируют
каждые 12 нед во время лечения и каждые 24 нед после его прекращения.
Наличие HBeAg и анти-НВе антител необходимо определять каждые 12—24 нед у
пациентов с HBeAg-положительным гепатитом. Наличие HBsAg контролируют
каждые 24—48 нед. Ретроспективный анализ пациентов, получавших пегИФН,
показал, что снижение титра HBsAg в первые 12—24 нед служит
прогностическим фактором долгосрочной вирусной супрессии и исчезновения
HBsAg [47]. Аналогично снижение титра HBeAg служило прогностическим
фактором его исчезновения для пациентов, у которых HBeAg до начала
лечения не выявлялся [48]. Эти данные свидетельствуют о том, что
контроль титра HBeAg или HBsAg может помочь в оценке продолжительности
терапии и выявлении пациентов с низкой вероятностью выявления
положительного эффекта в случае дальнейшего применения интерферона.
Однако данное предположение требует дополнительных исследований.
Пациенты, получающие терапию аналогами нуклеоз(т)идов, должны
проходить клинический осмотр каждые 24 нед, при этом подчеркивается
необходимость приверженности терапии. Уровень ДНК вируса гепатита В и
активность AJIT в сыворотке следует контролировать через 12 и 24 нед и
затем каждые 12—24 нед. У пациентов с субопти-мальным вирусологическим
ответом может быть получен положительный эффект в случае добавления
второго препарата. Такой подход основан на опыте применения ламивудина и
телбивудина — препаратов, характеризующихся более высокой частотой
развития устойчивости к ним. Между тем применимость такой стратегии и
критерии субоп-тимального ответа у пациентов, получающих энте-кавир или
тенофовир, не установлены. Определение HBeAg и анти-НВе антител следует
проводить каждые 24—48 нед у пациентов с HBeAg-положительным гепатитом
до начала лечения. У пациентов с HBeAg-отрицательным гепатитом уровень
HBsAg необходимо контролировать ежегодно. У пациентов, получающих
адефовир или тенофовир, необходимо контролировать уровень сывороточного
креатинина каждые 24 нед (или чаще, если речь идет о пациентах более
старшего возраста или повышенном риске развития почечной
недостаточности).
Когда можно прекратить лечение?
В идеале противовирусную терапию следует проводить до исчезновения
HBsAg. Однако вероятность этого события низка и составляет около 3—5%
через 3—5 лет терапии аналогами нуклеоз(т)идов и 5—10% через 5 лет
проведения курса терапии пегилированным интерфероном.
Пегилированный интерферон
ПегИФН назначают ограниченным курсом, поскольку его
иммуномодулирующие эффекты могут сохраняться и после прекращения
терапии. На основании результатов клинических исследований III фазы
рекомендуемая продолжительность терапии составляет 48 нед для пациентов с
HBeAg-положительным и HBeAg-отрицательным гепатитом. В настоящее время
проводятся исследования, которые позволят установить, достаточно ли
более короткого курса терапии для пациентов с HBeAg-положительным
гепатитом и такими «смягчающими обстоятельствами», как вирус с генотипом
А, высокая активность AJIT и низкий уровень ДНК вируса гепатита В.
Недавние исследования показали, что мониторинг титра HBsAg позволяет
выявить популяцию пациентов с медленным ответом, у которых может быть
получен положительный эффект от более длительной терапии, а также
пациентов, не отвечающих на лечение, продолжение которого становится
бесполезным. Но данный подход все еще требует подтверждения данными
новых исследований.
Аналоги нуклеоз(т)идов
Аналоги нуклеоз(т)идов назначают до достижения желаемой конечной
точки. Пациентам с декомпенсированным циррозом рекомендуется пожизненная
терапия в виду риска развития фатального обострения после ее отмены.
Пациентам с компенсированным циррозом некоторые эксперты также
рекомендуют проведение пожизненной терапии. Учитывая данные, указывающие
на обратное развитие фиброза или цирроза у пациентов с сохраняющейся
после 3—5 лет проведения противовирусной терапии вирусной супрессией,
можно рекомендовать прекращение терапии пациентам с подтвержденным
обратным развитием цирроза и исчезновением HBsAg (при условии
тщательного наблюдения и возможности немедленного возобновления терапии в
случае биохимического или клинического обострения).
Согласно клиническим рекомендациям Американской ассоциации по
изучению заболеваний печени (AASLD, Association for the Study of Liver
Diseases), у пациентов с HBeAg-положительным гепатитом без
прогрессирующего цирроза лечение следует продолжать до достижения
сероконвер-сии по HBeAg (HBeAg-отрицательный, анти-НВе антитела
положительные, ДНК вируса гепатита В в сыворотке не определяется) и
прекращать только после 6 мес проведения дополнительной терапии [8].
Многие эксперты подвергают сомнению валидность использования
сероконверсии по HBeAg в качестве терапевтической конечной точки,
ссылаясь на то, что у некоторых пациентов сохраняется виремия после
сероконверсии по HBeAg, а после прекращения лечения до 50% пациентов
вновь становятся HBeAg-положительными. Эти аргументы указывают на то,
что многие пациенты переходят в фазу неактивного носительства и остаются
в ней месяцами, годами и десятилетиями после сероконверсии по HBeAg.
Таким образом, прекращение терапии у пациентов, завершивших консолидацию
терапии после достижении сероконверсии по HBeAg, имеет смысл только в
том случае, если они продолжают наблюдаться.
Для пациентов с HBeAg-отрицательным гепатитом без прогрессирования в
цирроз терапевтическая конечная точка не установлена. Обострение нередко
возникает у пациентов, завершивших 2-летний курс терапии с
неопределимым уровнем ДНК вируса гепатита В в сыворотке, наблюдавшемся
на протяжении по крайней мере 1 года [49]. Предварительные данные,
полученные в одном небольшом исследовании, указывают на то, что среди 33
пациентов, прекративших терапию адефовиром (через 4—5 дет, с
неопределимым уровнем ДНК вируса гепатита В, по крайней мере, в течение 3
лет) у 18 отмечалась стойкая клиническая ремиссия, а у 9 исчез HBsAg на
протяжении в среднем 5 лет после отмены терапии [50]. При этом у всех
пациентов вскоре после прекращения лечения отмечался вирусологический
рецидив. Но в ходе последующего наблюдения (после отмены терапии)
уровень ДНК вируса гепатита В в сыворотке снижался до низкого или
неопределимого. Для подтверждения этих данных и выявления
прогностических факторов развития стойкой клинической ремиссии
необходимо проведение дополнительных исследований. Эта информация может
помочь в выборе пациентов, которым можно прекратить терапию, что избавит их от необходимости пожизненного приема препаратов.

 Парк Культуры
Парк Культуры